Сказать, что недавняя статья в Reuters о проблемах с регистрацией в Европе российской вакцины «Спутник V» вызвала бурю, значит, не сказать ничего. Продвигающий вакцину на мировой арене Российский фонд прямых инвестиций (РФПИ) мгновенно выпустил заявление о том, что статья «основана на ложных комментариях анонимных источников, является примером fake news и дезинформационной кампании против российской вакцины, организованной западным фармацевтическим лобби».
«РФПИ обратился в парижский офис Reuters с просьбой исправить многочисленные некорректные факты в статье», а также «провести внутреннее расследование в парижском офисе Reuters и принять меры против сотрудников агентства, распространяющих заведомо ложную и некорректную информацию», – говорилось в заявлении фонда.
Что именно имеется в виду под некорректными фактами, РФПИ не упомянул. Кое-что Reuters исправил, вставив дополнительные комментарии РФПИ. Но основа осталась прежней. Между тем в статье идёт речь не только о том, что Европейскому агентству лекарственных средств (EMA) якобы не были предоставлены отчёты о побочных эффектах вакцины.
Требования чистоты
Главное, что, как утверждают авторы статьи, согласно оценке французских учёных, работавших в Москве в связи с перспективами производства «Спутника» во Франции, создатели вакцины не смогли задокументировать соответствие так называемого главного банка клеток нормам ЕС.
«Четыре человека, знакомые с выводами французской делегации, заявили, что документы, рассмотренные учёными, показали: в культуре использовалась фетальная бычья сыворотка для выращивания основного банка клеток, а разработчики не задокументировали происхождение этой сыворотки», – говорится в статье.
«Фетальная бычья сыворотка широко используется во всём мире при разработке вакцин. Но после вспышки коровьего бешенства в 1980 годах регулирующие органы Европы и Северной Америки потребовали, чтобы разработчики вакцины документировали её происхождение из безопасного источника», – напоминают авторы.
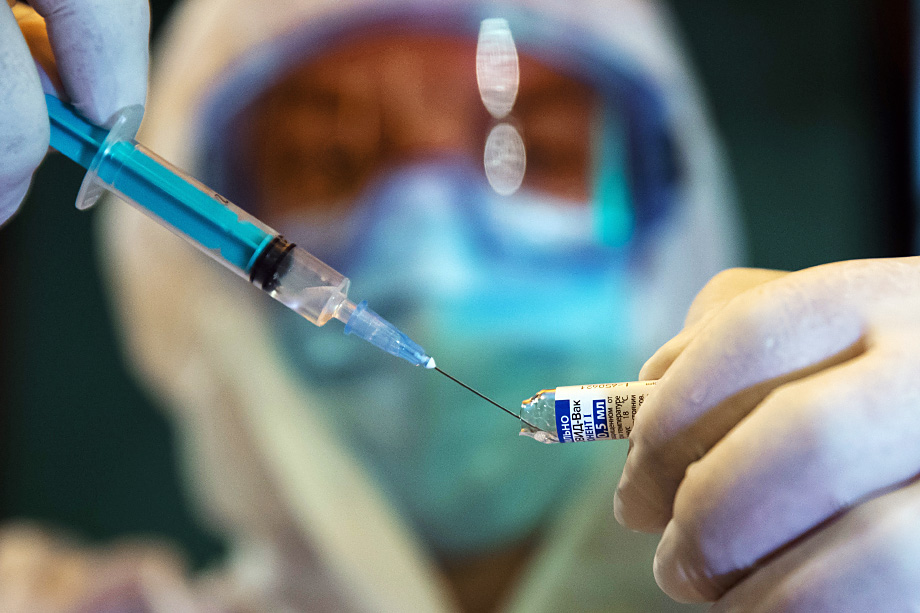 Согласно оценке французских учёных, создатели вакцины не смогли задокументировать соответствие главного банка клеток нормам ЕС.Фото: Сергей Мальгавко/ТАСС
Согласно оценке французских учёных, создатели вакцины не смогли задокументировать соответствие главного банка клеток нормам ЕС.Фото: Сергей Мальгавко/ТАСС
То есть они довольно откровенно намекают на использование в вакцине сыворотки крови телят, имеющей неизвестное происхождение, и на то, что она может стать источником прионной инфекции. Все известные прионные заболевания, объединяемые под названием «трансмиссивные губчатые энцефалопатии», неизлечимы и смертельны. Кроме того, они чрезвычайно трудно поддаются эпидемиологическому контролю и могут проявляться через годы после заражения. Самая распространённая из них – болезнь Крейтцфельдта – Якоба – начинает проявляться, как пишут специалисты, лишь спустя 12,5 года после внутримышечного введения инфицированных лекарственных препаратов, в том числе содержащих бычий тромбин гемостатиков. Именно поэтому в отношении банков клеток в Европе выработаны строгие правила безопасности.
По данным французской делегации, РФПИ заявил, что «сотовый банк “Спутник V” полностью соответствует всем требованиям EMA».
В обновлённом варианте всё той же статьи Reuters, который вышел уже после протестов РФПИ, уточняется, что, по данным РФПИ, институт Гамалеи «никогда не использовал для приготовления главного банка клеток “непрослеживаемую бычью сыворотку”». Кроме того, РФПИ добавил, что чистота банка клеток «Спутник V» от прионов была «подтверждена независимо». Тем не менее, кем и когда была произведена проверка, РФПИ Reuters так и не сообщил.
На аналогичный вопрос «Октагона» РФПИ ответил, что «вся информация по MCB (Master Cell Bank – главному банку клеток. – τ.) была предоставлена институтом Гамалеи российскому и международным регуляторам, которые подтверждают возможность его использования».
Вопросы репликации аденовируса
Таким образом, этот вопрос остаётся открытым до появления документов о проведении независимых проверок. Ровно также обстоят дела с потенциальной возможностью репликации аденовируса, которая, как следует из статьи, стала причиной апрельского скандала с отказом бразильского регулятора Anvisa от импорта «Спутника».
Anvisa публично заявила, что существует риск репликации используемого в «Спутнике» аденовируса, что потенциально может вызвать негативную реакцию у прививающихся.
По словам бывшего министра науки Серджио Резенде, консультирующего бразильских губернаторов штатов, которые хотят импортировать вакцину, российская сторона, похоже, была не знакома с требованиями бразильских регуляторов, но в конце концов она согласилась по его рекомендации переработать заявку на одобрение препарата.
«Anvisa сообщила, что исследования и документы, предоставленные институтом Гамалеи, указывают на “наличие репликации аденовирусов” и не дают адекватной оценки взаимосвязи между этим и безопасностью вакцины. Anvisa добавила, что условия, которые она предъявила, включали демонстрацию отсутствия репликации во всех партиях, отправленных в Бразилию».
Фрагмент статьи Reuters
То есть, несмотря на заверения РФПИ, что «ни в одной из производимых серий вакцины “Спутник V” не было обнаружено ни одного репликационно-компетентного аденовируса (RCA)», бразильцы от своих претензий не отказались и принимают каждую партию вакцины при условии доказательства отсутствия репликации в ней аденовируса.
Как утверждает молекулярный биолог Ирина Якутенко, «в редких случаях аденовирусы могут вернуть себе эту способность, позаимствовав необходимые генные фрагменты из клеток, в которых их наращивают для создания вакцин (это не обычные человеческие клетки, а специальным образом модифицированные). Это очень редкое событие, но, учитывая объемы производства, очевидно, что оно иногда происходит просто по законам больших чисел».
Кроме того, по её мнению, даже наличие некоторого количества размножающихся аденовирусов не представляет какой-либо опасности. «Даже если допустить обоснованность сомнений, в нынешней ситуации по-прежнему вакцинация даже вакциной с небольшим количеством реплицирующихся аденовирусов является несомненным благом», – считает она.
 РФПИ сообщает, что отсутствие в «Спутнике» RCA подтверждается двухуровневой системой тестирования – лабораторией института Гамалеи и лабораторией Росздравнадзора.Фото: Пётр Ковалёв/ТАСС
РФПИ сообщает, что отсутствие в «Спутнике» RCA подтверждается двухуровневой системой тестирования – лабораторией института Гамалеи и лабораторией Росздравнадзора.Фото: Пётр Ковалёв/ТАСС
В то же время, как сообщили «Октагону» в РФПИ, отсутствие в «Спутнике» RCA подтверждается двухуровневой системой тестирования – лабораторией института Гамалеи, а также лабораторией Росздравнадзора:
– Ни в одной партии, прошедшей контроль, не было выявлено RCA.
Тем не менее Anvisa в июне разрешила поставки «Спутника» на определённых условиях. Импорт вакцины разрешен только с заводов «Фармстандарт-УфаВита» и «Генериум», причём контроль содержания реплицирующихся аденовирусов должен проводиться для каждой партии.
Вероятно, именно эти два обстоятельства, помимо политических причин, и стали для EMA поводом для затягивания регистрации российской вакцины. При этом, похоже, сам институт Гамалеи они не слишком смущают. На внутреннем рынке вакцины продвигаются в принудительном порядке. Более того, возглавляющий институт Александр Гинцбург объявил, что до 20 сентября должна начаться вакцинация подростков, несмотря на то, что исследования вакцины на детях от 12 до 17 лет начались только 5 июля и, как сообщалось, должны продлиться год.
